日本制药工业协会的《制药协会指南》指出,日本的新药研发能力为全球第3位,仅次于美国和欧洲。厚生劳动省相关数据显示,2010年~2015年(截止9月底)日本共公布726条审批信息,其中2014年审批数量最高,为141条。
日本是我们的邻国,其在二战后迅速崛起并逐渐发展成为发达国家,对我国具有借鉴作用。作为发达经济体,日本的医药创新能力尤其值得目前处于转型中的国内医药行业学习。
日本的医药行业并非一开始就风调雨顺,在战后百废待兴之际,日本政府通过采取积极引导和重点扶持的强制干预措施实现了对医药产业的创新升级。如战后针对国内低迷的医药产业,制定了“引进、改良、模仿、吸收、自主开发”的创新策略,采取各种措施引进世界上最先进的技术并加以改造,并使其在二十世纪七八十年代便进入了创新的高峰期,为日本成为世界医药强国奠定了基础。近年来,随着日本医药产业创新技术不断完善,越来越多的日本医药企业如武田、第一三共、安斯泰来等,每年将销售额的10%~20%资金投入产品创新,使得企业逐渐成为创新体系中的主体,也使不少本土企业走出国门成为知名的跨国集团公司,从而享誉全球。
日本制药工业协会的《制药协会指南》指出,日本的新药研发能力为全球第3位,仅次于美国和欧洲。厚生劳动省相关数据显示,2010年~2015年(截止9月底)日本共公布726条审批信息,其中2014年审批数量最高,为141条。
图1 2010年~2015年(截止9月底)日本药物审批情况
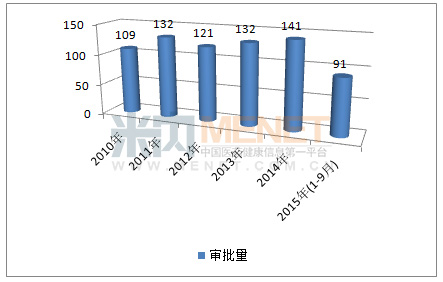
审批信息中有223条为增加适应症、修改说明书以及新剂型等相关信息,而其他503条为新批准的药物信息。在新获批批文中,获批较多依然是日本传统热点领域,如心血管、呼吸系统、代谢类及抗肿瘤药物等。而抗菌药及抗病毒类药物在近两年呈现快速上升势头,丙肝药如吉利德索菲布韦、Harvoni,艾伯维Viekirax;抗菌药如武田的术前杀菌剂Olanexidine、大冢抗结核药Delamanid,抗真菌药如日本科研株式会社的治疗灰指甲药Efinaconazole等等均获得批准上市,显示出日本企业跟踪全球研发热点的能力。
图2 2010~2015年批文获批较多的领域

由于日本拥有良好的创新环境以及其国人骨子里的“匠心”气质,吸引了全球制药巨头强生、拜耳、诺华、葛兰素、辉瑞、百时美施贵宝等,以及知名的仿制药企业迈兰等,还有罕见病制药名企健赞、夏尔等在日本设有其研发机构或分公司。通过分析2010~2015年间新获批药物的所属企业情况,笔者发现日本本土企业与外企基本保持均衡状态。而在治疗领域方面,本土企业在传统强项胃肠道及皮肤病等方面稍强于外企,但在抗艾滋病方面则弱于外企。
图3 日本药物获批企业格局情况

进口企业带进日本市场的药物,在上市时间上与欧美差距不是很大,显示出对日本市场的重视。如吉利德抗丙肝药索菲布韦、Harvoni的批准日期晚于FDA数月。而有些药物则优先在日本上市,如用于预防先天性FXIII亚基A缺乏症患者出血的药物,诺和诺德公司的重组凝血因子XIII NovoThirteen则先于其他发达国家选择在日本登陆;亚力兄公司的治疗低磷酸酯酶症药物STRENSIQ的5个规格的注射剂也率先在日本上市,且比FDA早获批3个月;而诺和诺德的胰岛素Ryzodeg在日本的获批时间更是比FDA批准时间早了3年;当然也有像胰岛素Victoza,其日本和FDA的审批时间基本同步的情况。
在血液制品领域,面对诺和诺德的强势来袭,本土企业并未示弱,2015年7月Kyowa Hakko Kirin的Acoalan(R) (抗凝血酶γ) 获得日本当局批准,用于治疗因先天性抗凝血酶缺乏和弥散性血管内凝血伴有抗凝血酶降低引起的血栓形成倾向。由于Acoalan为一种重组抗凝血酶制剂,因此将避免由人血引起的感染风险。
表1 2010~2015年外企在日本获批的部分药物情况
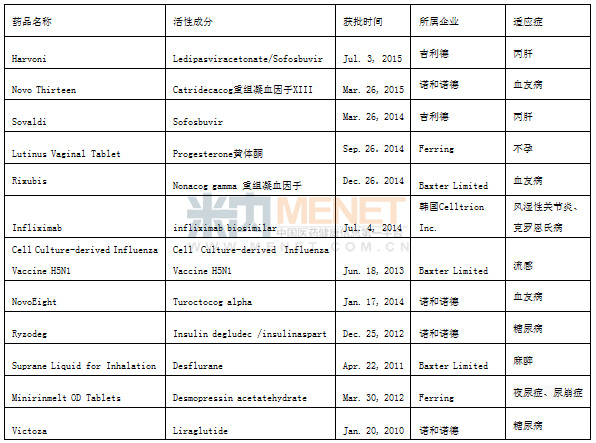
亚洲制药行业的领航者绕不过日本及印度两个邻国,印度主攻仿制药、而日本则偏于创新,因而他们中出现了不少具有国际视野的企业。作为全球制药企业TOP50的常客,日本的本土企业如武田、安斯泰来、第一三共、大冢、卫材、中外药业、住友、三菱田边以及协和发酵麒麟等享誉全球,这些企业每年的研发投入更是占其处方药销售的20%左右。源源不断的投入获得的是令人满意的回报,2010~2015年日本共批准234个新活性成分药物,其中本土企业占125个超过了外企;而在新批孤儿药数量方面,本土企业也不示弱,在其期间新获得批准的76个孤儿药中,本土企业占据38个,与外企平分秋色。
图4 2010~2015年批准的孤儿药情况
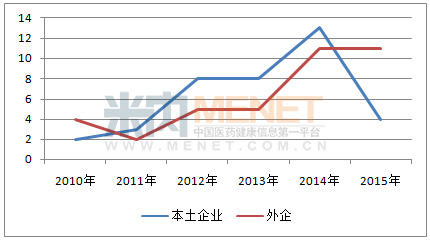
近年来中国游客疯抢日本药物屡屡登上新闻头条,《日本经济新闻》曾对访日外国游客进行调查发现:购买人数最多的是“药品和营养食品”。 中国国家旅游局的报告也称,访日中国游客购买的当地商品中,药品居首,其次是化妆品与婴儿用品。这或许从侧面提示了我们与这个邻居之间存在的巨大差距。



